Las enfermedades raras que más nos asustan a los padres son las que afectan a los recién nacidos. Muchas de ellas tienen un origen genético y nos hacen sentir culpables. El hiperinsulinismo congénito engloba a un grupo de síndromes que muestran una hipoglucemia prolongada debida a un exceso de producción de insulina que puede causar daño neurológico irreversible. Su diagnóstico se realiza muchas veces demasiado tarde, tras la muerte del bebé. La investigación en las bases moleculares de esta enfermedad abre un nuevo abanico de posibilidades diagnósticas y terapéuticas. La biología de sistemas es un enfoque prometedor, aunque aún en fase emergente.
Hiperinsulinismo congético
El hiperinsulinismo congético es una enfermedad rara con una incidencia de un caso por cada 40.000 nacidos vivos al año, aunque hay poblaciones con alta consanguinidad (como algunas regiones de Arabia Saudí y Finlandia) donde se da un caso por cada 3.000 neonatos [1]. Las bases genéticas de esta enfermedad todavía no están del todo claras, aunque se sabe que son heterogéneas, involucrando mutaciones dominantes y recesivas.
![Mecanismo de la secreción de insulina por las células betapancreáticas. Fuente: Fernández Lorenzo JR et al. [1]](https://rpni.sombradoble.es/wp-content/uploads/2014/06/Diapositiva2-300x287-300x287.jpg)
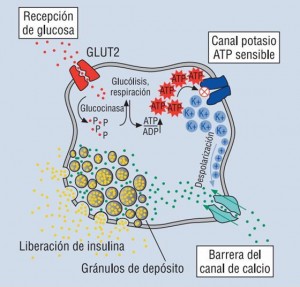
Mecanismo de la secreción de insulina por las células betapancreáticas. Fuente: Fernández Lorenzo JR et al. [1]
Se han observado casos que presentan mutaciones dominantes de los genes GCK y GLUD1 que codifican para la glucoquinasa y la glutamato deshidrogenasa, resp. La glucoquinasa controla la velocidad de glucólisis, fosforilando la glucosa a glucosa-6GP, incrementando el cociente ATP/ADP, lo que produce un cierre de los canales de potasio y la activación de los canales de calcio. La entrada de calcio al interior celular provoca la secreción de insulina. La glutamato deshidrogenasa incrementa la tasa de oxidación del glutamato en las células beta, lo que provoca un aumento de la secreción de insulina.
Además de los cuatro genes anteriores, se han observado casos con mutaciones en otros cinco genes (SLC16A1, Hadh, UCP2, HNF1A y HNF4A). No me extenderé en los detalles. Lo más importante a recordar es que estos nueve genes asociados al hiperinsulinismo congénito ayudan a entender sólo el 50% de los casos [2]. Las bases genéticas de esta enfermedad rara todavía guardan secretos por desvelar.
Biología de sistemas
La biología de sistemas o biología sistémica es el estudio integrado de las interacciones ómicas dentro de las células, es decir, las interacciones entre genes (genómica), proteínas (proteómica), factores de transcripción (transcriptómica), moléculas pequeñas o metabolitos (metabolómica) y demás componentes funcionales de la célula. La biología de sistemas estudia además su relación con los procesos fisiológicos y fisiopatológicos en los organismos vivos. La aplicación de la biología de sistemas a la medicina promete avances en nuestra comprensión de muchas enfermedades, incluidas las raras, y ha llevado a la emergencia de la así llamada medicina de sistemas o medicina en redes (network medicine).
![Esquema del análisis de redes biológicas basado en el interactoma y su modularización. Fuente: Stevens et al. [2].](https://rpni.sombradoble.es/wp-content/uploads/2014/06/Diapositiva31-232x300-232x300.jpg)
Esquema del análisis de redes biológicas basado en el interactoma y su modularización. Fuente: Stevens et al. [2].
Una herramienta básica en la biología de sistemas es el interactoma, que identifica de forma sistemática todas las interacciones entre las proteínas dentro de un organismo. En un contexto biomédico se utiliza el llamado diseasoma (diseasome), que combina todos los datos disponibles de asociaciones entre genes y patofenotipos (fenotipos asociadas a enfermedades).
Las enfermedades raras tienen un lugar especial en el diseosoma humano. Su tasa de prevalencia es baja, pero la mayoría están asociadas a genes esenciales para el organismo, mientras que los genes asociados a las enfermedades más comunes no suelen ser esenciales [3]. Además, la topología de las subredes de genes asociados a enfermedades raras presenta diferencias claras, lo que sugiere a algunos expertos que la topología del diseosoma puede ofrecer más información para estas enfermedades que para las convencionales.
El diseosoma humano completo todavía no se ha desarrollado. En el caso de las enfermedades endocrinas, cuyo patofenotipo suele variar mucho de un enfermo a otro y depende mucho de la historia clínica, se limita a un número reducido de enfermedades. Entre ellas, destaca el hiperinsulinismo congénito en la infancia.
Biología de sistemas en el hiperinsulinismo congénito
El fenotipo de esta enfermedad rara es muy heterogéneo, con gran variabilidad en el momento de presentación y en su evolución futura. En casi el 50% de los pacientes la hipoglucemia asociada se resuelve de forma espontánea en cuestión de semanas a meses tras el diagnóstico. En contraste con la enfermedad transitoria, la fisiopatología de la persistente está mucho mejor descrita.
![Red del interactoma humano asociada al hiperinsulinismo congético permanente. Fuente: Fuente: Stevens et al. [2].](https://rpni.sombradoble.es/wp-content/uploads/2014/06/Diapositiva4-214x300-214x300.jpg)
Red del interactoma humano asociada al hiperinsulinismo congético permanente. Fuente: Fuente: Stevens et al. [2].
En concreto, se ha asociado a la enfermedad dos redes de señalización celular. Por un lado la asociada a la tropomiosina, una proteína componente de los filamentos de actina en el citoesqueleto; de hecho, la insulina tiene efectos sobre la arquitectura estructural de la célula. Y por otro lado, la señalización nuclear que regula la proteína SMAD2, que está asociada con el desarrollo de islotes pancreáticos. Para explicar el papel exacto de estas asociaciones en la enfermedad se requiere una investigación futura específica.
Conclusiones
La biología de sistemas tiene un papel muy importante a la hora desvelar la fisiopatología de las enfermedades raras. El hiperinsulinismo congénito es un buen ejemplo. Aún así, todavía queda mucha investigación básica en biología de sistemas y en medicina de sistemas para que los primeros avances que se están realizando en la actualidad acaben conduciendo a nuevas técnicas de diagnóstico y tratamiento de las enfermedades raras.
Referencias
[1] J. R. Fernández Lorenzo et al., “Perspectivas actuales en el tratamiento del hiperinsulinismo congénito,” Acta Pediátrica Española 67: 103-111, 2009. http://goo.gl/tB49Gg [2] A. Stevens et al., “Network analysis: a new approach to study endocrine disorders,” Journal of Endocrinology 52: R79-R93, 2014. http://goo.gl/zXa1Ww [3] M. Zhang et al., “The Orphan Disease Networks,” The American Journal of Human Genetics 88: 755-766, 2011. http://goo.gl/MgfhPxAutor
Este artículo ha sido escrito por Francisco R. Villatoro (profesor de la Universidad de Málaga y autor del blog La Ciencia de la Mula Francis), como colaboración con Raras pero no invisibles. Podéis seguirlo en @emulenews
Pero congenito no quiere decir que lo tiene la mama o el papa mi hija murio de esta maldita enfermedad hace 14 años con tres meses de vida vivimos en España despues tuve dos ninos y dando gracias a dios estan bien un saludo y mucho ánimo para toda esta gente